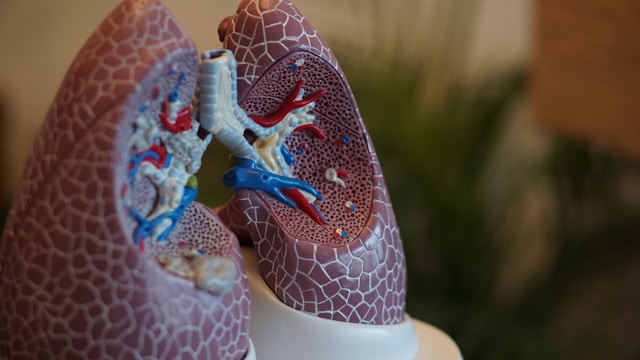
COPD steht für die englische Benennung „Chronic Obstructive Pulmonary Disease“ und ist eine nicht-heilbare, dauerhafte, atemwegsverengende Lungenerkrankung. Etwa 10% der erwachsenen Bevölkerung ist an COPD erkrankt, Tendenz steigend.1 COPD ist die 3. häufigste Todesursache weltweit.3 Dadurch kann man sagen, dass diese Krankheit ein globales Gesundheitsproblem ist.
Anatomie
Die Lunge besteht aus einem rechten und linken Lungenflügel. Der rechte Lungenflügel wird als drei Lungenlappen gebildet und der linke Lungenflügel aus zwei Lungenlappen, damit das Herz noch genug Platz hat.
Wenn man das Bild hier unten über Kopf betrachtet, ist die Lunge aufgebaut wie ein umgedrehter Baum. Die Luftröhre (auch Trachea genannt) bildet den Stamm und von ihr gehen zwei Hauptäste ab, die Bronchien. Diese sind noch in kleinere Äste und Zweige unterteilt und enden mit Alveolen (die Lungenbläschen) die wie Trauben an einer Rebe angeordnet sind. Die 200 – 300 Millionen Lungenbläschen pro Lunge sind mit kleinen Wegen miteinander verbunden und mit einem Netz als Haargefässe überzogen.
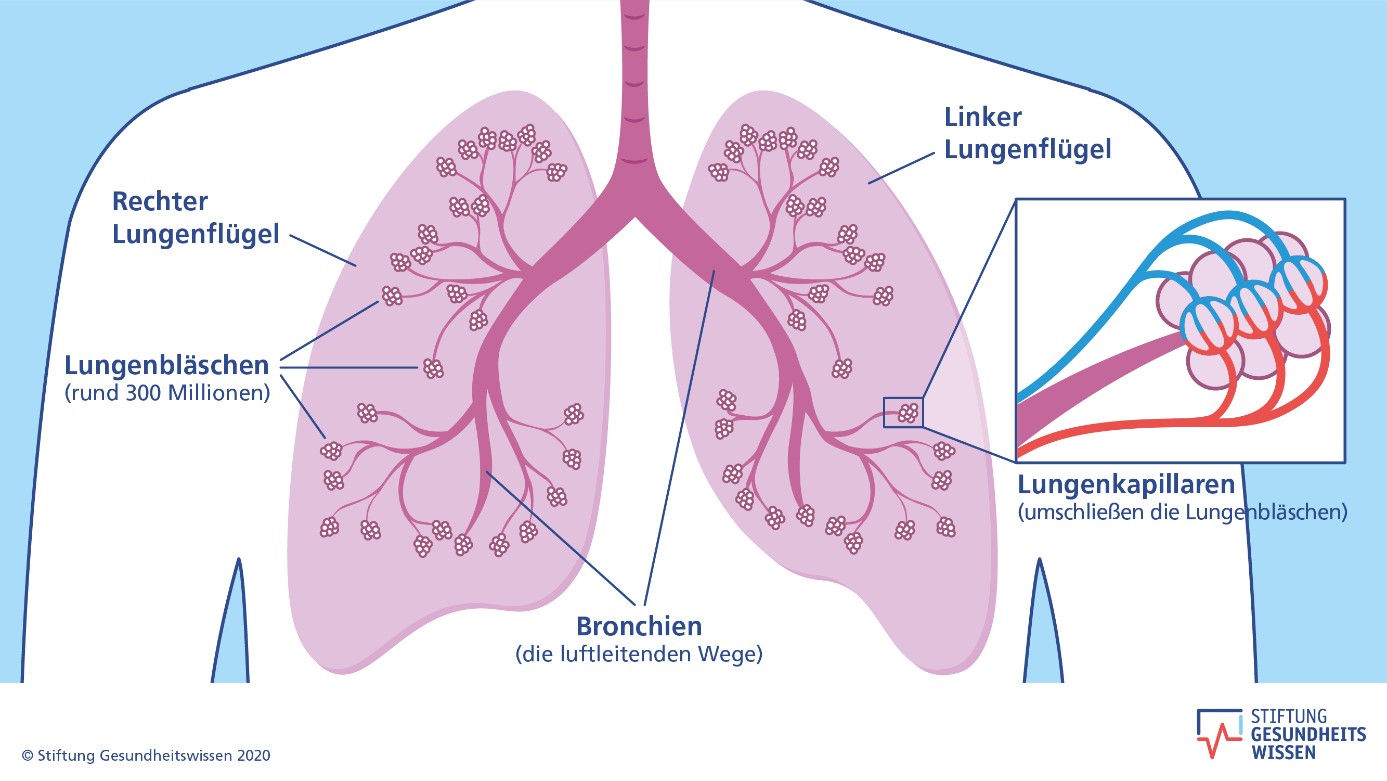
Quelle: Stiftung Gesundheitswissen
Die Hauptfunktion der Lunge besteht darin, dass es das Zielorgan der Atmung ist. Hier findet der Gasaustausch statt. Die Atmung wird jedoch nicht allein von der Lunge durchgeführt, sondern hauptsächlich von anderen Strukturen:
- Der Brustkorb dient als Schutz der Lunge. Er ist sein bewegliches Gerüst. Ebenfalls wichtig ist die Kraftübertragung während der Atmung. Die Rippen und das Brustbein heben und senken sich bei der Atmung.
- Die Atemmuskeln bewegen den Brustkorb bei der Atmung. Bei verminderter Kraft und Ausdauer der Atemmuskeln, verringert sich das Atemzugvolumen und Atemminutenvolumen.
- Der wichtigste Atemmuskel, das Zwerchfell (oder auch Diaphragma genannt), bewegt sich bei jedem Atemzug in Optimalfall 10 – 12 cm.
- Andere Atemhilfsmuskeln sind verschiedene Inspirationsmsukeln (Inspiration = Einatmung), die bei der Einatmung helfen, indem sie den Brustkorb anheben. Diese befinden sich and er Rückseite des Brustkorbes. Zudem helfen die Expirationsmuskeln (Expiration = Ausatmung) dabei, den Brustkorb wieder zusammenzuziehen und befinden sich an der Vorderseite des Brustokorbes.
Gasaustausch
In den Haargefässen findet der Austausch von Sauerstoff aus den Lungenbläschen und CO2 aus den Blutgefässen statt. Der Sauerstoff aus der eingeatmeten Luft strömt durch die Lungenbläschen und Kapillaren ins Blut ein und bindet sich dort an den Sauerstoff in den roten Blutkörperchen. Von da aus wird der Sauerstoff weitergeleitet, zu den Stellen im Körper, die konstant mit Sauerstoff versorgt werden (Muskeln, Gehirn, etc.). Im Austausch nimmt es Abfallstoffe auf, am wichtigsten CO2, welche wieder an die roten Blutkörperchen gebunden, zurück zur Lunge gepumpt werden und von dort aus dann abgeatmet werden können.
Durch die Atmung werden essentielle Stoffwechselprogramme durchgeführt, die für unsere Körperfunktionen überlebenswichtig sind. Der Gasaustausch ist ein wichtiger Bestandteil für die Energiegewinnung im Körper sowie für die Zellatmung.
Wie entsteht die Problematik?
Auf der Abbildung hier unten sind eine gesunde Lunge und eine an COPD erkrankte Lunge im Vergleich dargestellt. Die Erkrankung umfasst in der Lunge hauptsächlich die kleinen Atemwege und die Lungenbläschen. Hier ist eine durchgehende Entzündung zu beobachten und ein Ungleichgewicht zwischen Ein- und Ausatmung, welches zu oxidativem Stress führt. Oxidativer Stress ist eine Stoffwechsellage, bei der es zu Schäden von Zellen oder deren Funktionen kommt
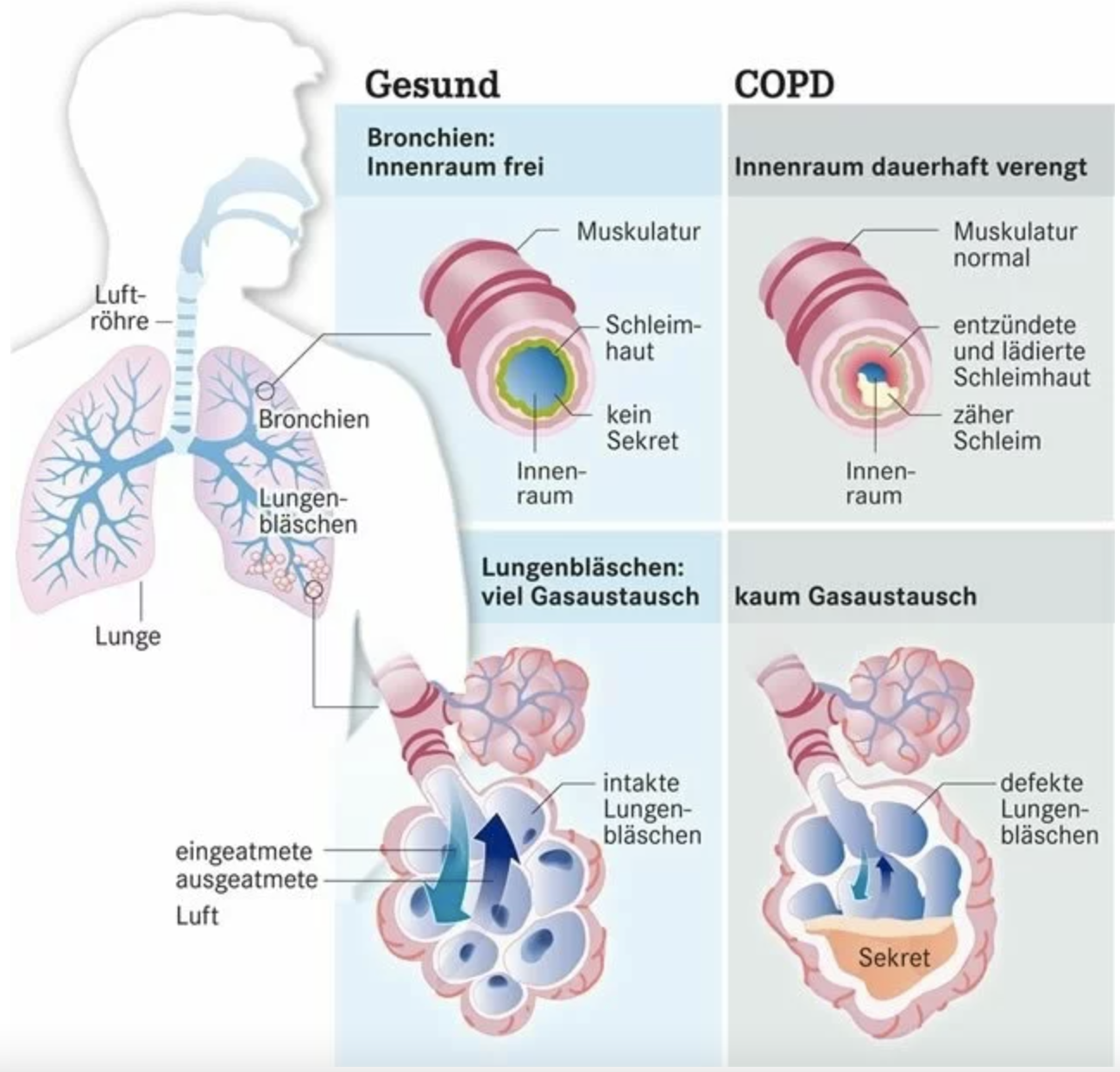
Die Schleimhäute und Schleimdrüsen sind chronisch entzündet, nehmen an Grösse zu und starten eine Überproduktion von Schleim. Des weiteren wird die oberste Schicht der Lungenbläschen verletzt. Im Laufe der Erkrankung nimmt die Elastizität des Lungengewebes ab und die Flimmerhärchen verlieren ihre Beweglichkeit. Hierdurch wird der elastische Rückstoss-Druck in der Lunge reduziert, der dafür wichtig ist, dass die Lunge beim Ausatmen nicht kollabiert. Die Atemwege verengen sich, die Atmung verringert sich und die Luft bleibt in den Lungen eingeschlossen. Dies wird auch „Trapped Air“ genannt.
Diese Veränderungen der Lunge und Atemwege setzt sich weiter fort. Man spricht von einer Lungenfibrose: Das funktionierende Lungengewebe wird schrittweise ersetzt durch funktionsloses Bindegewebe, welches man mit Narbengewebe vergleichen kann. Dadurch sind die Veränderung in den Atemwegen dauerhaft und unumkehrbar.
Trotz Medikamente die die Bronchien erweitern herrscht ein vergrösserter Atemwiderstand und wir die Atmung zunehmend erschwert. Fortschreitend reduziert sich die Oberfläche der Lungenbläschen. Diese werden zwar grösser, verschmelzen jedoch miteinander. Nun ist zu sprechen von einem Lungenemphysem. Der Gasaustausch kann nicht mehr uneingeschränkt stattfinden und die Atmung gerät zunehmend in ein Ungleichgewicht. Dies äussert sich dadurch, dass der Druck der Ausatemluft weniger wird als Atemwiderstand der verengten Gefässe und die Ausatmung erschwert wird. Hierdurch wird nicht die ganze Luft ausgeatmet und es kommt zu einer Hyperinflation (Lungenüberblähung). Dies ist der Hauptgrund für die Kurzatmigkeit und die somit niedrige Lebensqualität.
Der Verlauf der Erkrankung ist zunehmend schlechter und geht einher mit verschiedenen Folgekrankheiten. Zudem können Exazerbationen auftreten. Exazerbationen sind akute Verschlechterungen des Gesundheitszustandes und des Krankheitsverlaufes. Diese werden meist ausgelöst durch virale oder bakterielle Infektionen oder andere Umwelteinflüsse. Exazerbationen sind zu erkennen an starker Symptomverschlechterung, die meist 7 – 10 Tage anhalten. Ab einer Dauer von 8 Wochen rehabilitieren 20% der Patienten nicht mehr zu ihrem vorherigen Status. 13 Die Symptome können sich äussern in einer erhöhten Atemwegsentzündung, erhöhten Schleimproduktion, Air Trapping (Luft bleibt in den Lungen eingeschlossen und kann nicht ausgeatmet werden) und erhöhter Atemnot. 4 Exazerbationen lassen sich einteilen in mild, moderat (Behandlung durch Medikamente) und schwer (Behandlung stationär). Ist eine stationäre Behandlung notwendig oder die Häufigkeit von Exazerbationen bei 2 oder mehr pro Jahr, dann haben diese Patienten eine schlechtere Lebenserwartung. 14
COPD ist eine systemische Krankheit. Das heisst dass nicht nur lokal in der Lunge Probleme entstehen, sondern dies Auswirkungen hat auf den kompletten Körper. Daher steigt wie Wahrscheinlichkeit immens, verschiedenen Nebenerkrankungen zu entwickeln. Die häufigsten werden hier aufgelistet, da es wichtig ist, dass diese erkannt und behandelt werden und auch für unsere Therapie eine grosse Rolle spielen.
Durch ein Ungleichgewicht zwischen Energieaufnahme und -verbrauch geht COPD mit starkem Gewichtsverlust und Abbau von Muskelmasse einher. Durch ständig anhaltende Entzündungsprozesse wird der Appetit gedrosselt und der Ruheenergieumsatz erhöht. Des weiteren wird der Muskelstoffwechsel negativ beeinflusst, wodurch das Gleichgewicht zwischen Regeneration und Zelltod gestört ist und es zu Veränderungen der Muskelfasern kommt. Die Muskulatur verliert an Ausdauer und des Zwerchfell an Kraft. Für dasselbe Ausmass an körperlicher Belastung, brauchen COPD Erkrankte mehr Energie als gesunde Menschen und ist der Aufbau von Muskelmasse und Kraft schwieriger. 30
Das Air Trapping (Restluft in der Lunge) und dadurch ständige Druckschwankungen, können Auswirkungen auf das Herz- Kreislaufsystem haben. Der diastolische Druck (Druck auf die Gefässe, wenn der Herzmuskel erschlafft) wird beeinflusst und dadurch die Anspannung der Herzkammern, was Herzinfarkte stimulieren kann.
Durch die Lungenüberblähung wird das Zwerchfell nach unten gedrückt und es kommt zu einem Zwerchfelltiefstand. Der wichtigste Atemmuskel kann sich nicht mehr so gut bewegen und vor allem nicht mehr gut Luft ziehen. Die restlichen Atemhilfsmuskeln müssen mehr Arbeit leisten und werden überlastet. Dies kann zu verschiedenen Beschwerden im Oberkörper führen.
Bei COPD entstehen oft muskuläre Dysfunktionen. Vor allem im Hüft-, Oberschenkel- und Armmuskulatur ist hiervor betroffen. Es kommt zu schneller muskulärer Ermüdung, wodurch die Kurzatmigkeit verstärkt werden kann. Es entsteht eine Änderung der Muskelfaserverteilung, was zu mehr oxidativer Stress und entzündlichen Veränderungen der Muskulatur führt. 27 Hierdurch kann sich eine Insulinresistenz entwickeln, und somit eine vergrösserte Wahrscheinlichkeit auf Diabetes. Darüber hinaus ist bekannt dass fast 70% aller COPD Patienten Osteoporose bekommen und auch Depressionen gehören zu den weit verbreitete Folgen einer COPD Diagnose.
Risikofaktoren
Die Risikofaktoren für die Entstehung von COPD nehmen in den letzten Jahren zu. Dies hat damit zu tun, dass die Bevölkerung immer älter wird, die Zahl an Infektionen und kardiologischen Erkrankungen (eine Gruppe verschiedener Erkrankungen, die meist chronisch verlaufen und das Herz und die Blutgefässe betreffen), Bewegungsarmut und auch der Konsum von Tabak steigen. Es gibt sowohl Risikofaktoren, die man selbst beeinflussen kann, als auch Risikofaktoren, die weniger gut beeinflussbar sind.
Rauchen ist der grösste Risikofaktor für die Entwicklung von COPD, darunter gehört nicht nur das Rauchen von Zigaretten, sondern auch Zigarren und Wasserpfeife oder auch das Passivrauchen.3
Hierneben spielt die Genetik eine weitere wichtige Rolle. Eine schlechte Lungenentwicklung (tritt auf bei 4 – 12 % der Menschen) und niedrige Lungenfunktion in jungem Erwachsenalter bilden einen weiteren Risikofaktor. Es wurde herausgefunden, dass bei 50% der Patienten mit COPD, sich die Krankheit aufgrund von abnormalem Lungenwachstum entwickelt. 3
Normal entwickelt sich die Lunge und hat ihren Höchststand der Entwicklung und Funktion im Alter von 25 Jahren. Dann erreicht die Lungenfunktion ein Plateau und wird mit zunehmendem Alter langsam schlechter. Umwelteinflüsse in jeder dieser Phasen haben positive oder negative Auswirkungen auf diese Kurve. 1, 4 So sind zum Beispiel der Alkoholkonsum unter 15 Jahren und Rauchen in der Schwangerschaft bekannt dafür, das Immunsystem, Lungenwachstum und -entwicklung negativ zu beeinflussen. 4
Ein weiteres Risiko besteht im Einatmen von chemischen Partikeln, wie Substanzen die frei werden während Holzverbrennung, Düngerverwendung, Arbeiten mit Asbest oder viel Staub. Auch die Luftverschmutzung in Innenräumen durch Öfen, Heizen und Kochen mit Biomasse 4, ist besonders in Entwicklungsländern ein grosses Thema. 3
Die gesundheitliche Vorgeschichte eines Menschen spielt zudem eine grosse Rolle. Die Anwesenheit von von den folgenden Faktoren können das Risiko auf die Entstehung von COPD erhöhen: 1
- Asthma 5
- Allergien
- Tuberkulose
- HIV-Infektion
- häufiges Auftreten von Sinusitis (Nasennebenhöhlenentzündung) oder Lungenentzündungen
- Übergewicht und Obesitas
- Ernährung (zuckerhaltig, wenig Obst und Gemüse)
- Anwesenheit von Depressionen
- Bluthochdruck
- hohe Entzündungswerte
- weniger als 60 Minuten körperliche Aktivität pro Tag im Alter zwischen 60 – 85 Jahren
- Diabetes oder (periphere) Durchblutungsstörungen
Bei mehreren Risikofaktoren hat man einen verhältnismässig grossen Einfluss, diese Risikofaktoren zu minimieren, durch einen gesunden Lebensstil mit gesunder Ernährung, Sport und Bewegung. Hierdurch wird das Risiko an Übergewicht, Infektionen, Depressionen, Bluthochdruck, hohe Entzündungswerten und Diabetes minimiert und somit sinkt auch das Risiko, an COPD zu erkranken.
Das Problem unserer Gesellschaft
Dass unsere Gesellschaft immer ungesünder lebt, muss mittlerweile nicht mehr diskutiert werden. Wo man vor 100 Jahren noch 20 Kilometer am Tag gelaufen ist, läuft der Mensch heutzutage im Durchschnitt nur noch 800 Meter am Tag. Dies hat sich während des Lockdowns noch einmal reduziert auf nur noch 200 Meter täglich. Ernährungstechnisch ist die Lage ähnlich: Dort, wo in Deutschland vor 160 Jahren im Durchschnitt 2120 Kalorien täglich konsumiert wurde, liegen wir heutzutage bei 3.539 Kalorien pro Tag. In Zahlen ausgedrückt bedeutet dies, wir haben die Energiezufuhr um 166% gesteigert obwohl wir uns zu 96% weniger bewegen.

Symptome
Die wichtigsten COPD-Symptome sind: 1, 4
- Kurzatmigkeit. Häufig findet mit der Zeit eine progressive Verschlechterung statt. Die Kurzatmigkeit ist persistent anwesend und wird schlechter bei Anstrengung. Oft ist vor allem das Ausatmen erschwert.
- Chronischer Husten. Das Husten ist oft nicht-effektiv. Es findet ein schlechtes Abhusten statt und es gibt Schwierigkeiten Schleim zu entfernen.
- Brustkorb Steifheit. Bei COPD entsteht oft ein Haltungsverfall und entwickelt sich eine sogenannter Fassthorax. Als Fassthorax bezeichnet man einen kurzen und breiten, fassförmigen Brustkorb (Thorax), der in der Inspirationsstellung (Einatmungsstand) fixiert ist.
- Bei Patienten mit COPD entsteht mit der Zeit oft ein Gewichtsverlust, eine allgemeine Müdigkeit und geringe Belastbarkeit.
Diagnose
Um COPD zu diagnostizieren, wird die medizinische Vorgeschichte des Patienten im Hinblick auf Risikofaktoren zusammengetragen. Diese Auflistung enthält Folgendes: 4
- Anwesenheit von Risikofaktoren und schädliche Umwelteinflüssen
- medizinische Vorgeschichte in Bezug auf Asthma, Allergien, Sinusitis, Polypen, Atemwegsinfektionen in der Kindheit und andere chronische Atemwegserkrankungen oder chronische Erkrankungen
- Familiengeschichte COPD oder andere chronische Atemwegserkrankungen
- Entwicklung und Abhängigkeiten der Symptome
- Exazerbationen (Verschlimmerungen, hierzu folgen noch weitere Informationen) oder Krankenhausaufenthalte aufgrund von Atemwegsbeschwerden
- Nebendiagnosen sowie kardiologische Erkrankungen, Osteoporose, muskuloskeletale Probleme
- Impat der Krankheit auf den Alltag, Einschränkungen in Aktivitäten und Partizipationen, Sorgen und Ängste
- Soziales Umfeld, familiäre Unterstützung
- Möglichkeiten und Ressourcen die Risikofaktoren zu minimieren
Die Anwesenheit von den oben aufgelisteten Symptomen und Risikofaktoren ersetzt nicht die weitere Diagnostik, erhöht aber die Wahrscheinlichkeit eine Diagnose von COPD. Der Lungenfacharzt kann einen Lunenfunktionstest, eine sogenannte Spirometrie, durchführen, um zwei bestimmte Werte zu untersuchen. Bei einer Atemwegseinschränkung müssen diese beiden Werte vermindert sein:
- FEV1. Das Lungenvolumen, das man innerhalb von einer Sekunde ausatmen kann.
- FVC. Das totale Lungenvolumen eines gesamten Ausatemzuges nach maximaler Einatmung.
Ziel der Untersuchungen ist, den aktuellen Status der Atemeinschränkung zu messen und den Impakt der Krankheit auf den allgemeinen Gesundheitszustand des Patienten zu erfahren. Hierdurch kann eine Risikoeinschätzung von zukünftigen Events wie Exazerbationen (Verschlimmerungen), Krankenhausaufenthalten und Prognose der Lebenserwartung gemacht werden. Ausserdem ist es wichtig, begleitende Erkrankungen zu untersuchen und behandeln. Hierzu erfahren sie später noch genauer, welche Krankheiten oft in Verbindung mit COPD stehen.
Weitere zusätzliche diagnostische Mittel können helfen, andere Krankheiten auszuschliessen oder dabei unterstützen, die richtige Therapie bei COPD zu finden:
- Röntgen- oder CT-Untersuchung vom Brustkorb
- Finger Pulsoximeter zur Ermittlung der Sauerstoffsättigung im Blut
- Blutsauerstoff Messung eines Blutgefässes
- Peak-Flow Messung zu Bewertung von Atemnot
- Belastungstests
- Blutbild
Mythen
Nur Raucher bekommen COPD
Epidemiologische Studien zeigen, dass 65% der COPD Patienten auf der Welt keine Raucher sind.2, 3 Rauchen ist zwar der grösste und schwerwiegendste Risikofaktor für die Entstehung von COPD, jedoch müssen auch die anderen Faktoren in Betracht gezogen werden.
Im Vergleich zu nicht-Rauchern, die an COPD erkranken, haben Raucher stärkere Symptome und einen schwereren Krankheitsverlauf und ein höheres Risiko auf systemische Entzündungen, Lungenkrebs und Herz- Kreislauferkrankungen, welches bei nicht-Rauchern nicht der Fall ist. 4 COPD Erkrankte, die Raucher sind, haben ausserdem eine höhere Sterberate.
Wenn man schon COPD hat, lohnt es sich nicht mehr, mit dem Rauchen aufzuhören.
Langzeit Studien zeigen, dass das Aufhören zu Rauchen auf lange Sicht den Krankheitsverlauf um 25% verbessern kann. 7
COPD Patienten dürfen keinen Sport machen und sollen körperliche Anstrengung vermeiden
Die Schäden an der Lunge können durch Sport nicht behoben oder verbessert werden. Sport ist jedoch wichtig, um den Verlauf der Krankheit zu begünstigen und Verschlechterung zu verlangsamen. Des weiteren können dadurch Symptome gelindert werden und die Lebensqualität gesteigert werden. Wie dies genau abläuft, erläutern wir hier.
Asthma und COPD ist das Gleiche
In manchen Patienten koexistieren Asthma und COPD. Hierfür gibt es Benennungen wie Asthma-COPD Overlap Syndrom (ACOS). 4 Die beiden Krankheiten haben gemeinsam, dass es sich um eine chronische Atemwegserkrankung handelt, jedoch sind es definitiv zwei eigenständige und unterschiedliche Krankheiten.
Häufig gestellte Fragen
Kann ich trainieren trotz Sauerstoffgerät
Eine Sauerstoffsupplementierung mittels eines mobilen Sauerstoffgerätes ist für das Training kein Hindernis. Es kann sogar die Leistung steigern und dadurch kann eine höhere Trainingsintensität ermöglicht werden. 15
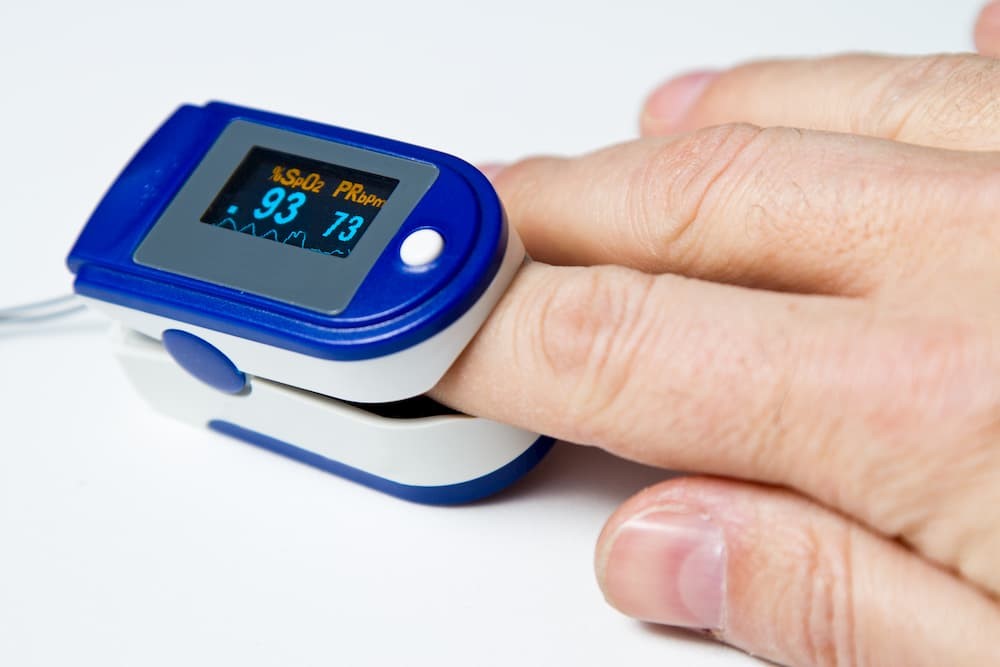
Gebrauch eines Pulsoximeters
Ein Pulsoximeter (siehe Bild unten) misst den prozentuellen Sauerstoffgehalt im Blut. Dies geht ganz umkonpliziert am Zeigefinger. Der Wert ist gut zu gebrauchen zur Überwachung bei z.B. körperlicher Aktivität und/oder Training.
Eine optimale Sauerstoffsättigung bei einem gesunden Erwachsenen liegt zwischen 95 und 100%. Sollte die Sättigung unter 90% gelangen, sollte man entweder die Belastung und Trainingsintensität vermindern oder die Pausen verlängern. Bei einer Sättigung unter 88% sollte die Belastung abgebrochen werden.
Vor einer weiteren Belastung sollte der Wert wieder bei über 90% oder optimal über 95% sein. Wenn nach 2 – 3 Minuten keine Aufsättigung stattgefunden hat, sollte man die Belastung / Training abbrechen. Ist unter Belastung keine Sauerstoffsättigung von über 90% möglich, sollte die Belastung / das Training unter Sauerstoffgabe erfolgen.
Was können Sie als Patient oder Arzt bei/von uns erwarten?
Physiotherapeutische Massnahmen tragen sowohl präventiv als auch zur Symptomlinderung, Verbesserung der Lebensqualität und der Lebenserwartung einen sehr wichtigen Teil zur Behandlung bei.
Wie bei jedem unserer (neuen) Patienten, erwartet sie zu Beginn der ersten Therapiesitzung ein ausführliches Anamnesegespräch, indem wir die gesundheitliche Vorgeschichte, die anwesenden Risikofaktoren und Nebendiagnosen, den Krankheitsverlauf und den Impakt der Erkrankung auf das alltägliche Leben erfahren möchten. Hierfür können folgende Fragenlisten ausgefüllt werden und einen guten Eindruck davon geben:
- Modified British Medical Research Council Questionnaire (4)
Zudem wird gemeinsam mit dem Patienten ein individuelles Anforderungsprofil erstellt, welches speziell auf die alltäglichen Anforderungen im Leben des Patienten abgestimmt wird. Ziel davon ist es, einen klar objektiv definierten IST- Standpunkt zu gestalten und eine erste Planung für den zu erreichenden Soll-Zustand zu formulieren. Dieser Weg wird durch den Transfer der Therapie stattfinden und laufend neu monitorisiert und evaluiert, um zu jedem Zeitpunkt über den aktuellen Leistungszustand des Patienten Bescheid zu wissen.
Um diese Art der Methodik noch effizienter und das volle Potenzial aus der Behandlung schöpfen zu können, bieten wir Ihnen die Möglichkeit der erweiterten Therapiezeit auf Selbstzahler-Basis an. Ziel dessen ist es, unser Behandlungspotential voll auszuschöpfen, eine qualitativ hochwertige Therapie zu garantieren und damit das Therapieergebnis zu optimieren. Durch die verlängerte Zeit können unsere Therapeuten noch effizienter am Therapieprozess arbeiten.
Um den IST-Standpunkt des Patienten zu messen und im Laufe der Behandlung zu evaluieren werden am Anfang der Behandlung und zur Evaluation im weiteren Behandlungsverlauf verschiedene Assessments gemacht. Um die Belastungstoleranz zu bestimmen, können der „6 Minuten Gehtest“ und der „Sit to Stand Test“ ausgeführt werden.
- Beim 6 Minuten Gehtest, wird die maximal erreichte Distanz innerhalb von 6 Minuten gemessen.
- Beim Sit to Stand Test werden die korrekt ausgeführten Aufstehwiederholungen von einem Stuhl innerhalb eines definierten Zeitintervalls von 30 oder 60 Sekunden gezählt. Hier kann man ebenfalls die Zeit messen, die der Patient für die Durchführung von X Wiederholungen braucht.
Um die Muskelfunktion zu prüfen und zu evaluieren können auch gesonderte Krafttests gemacht werden für die verschiedenen Muskelgruppen. Hier kan man messen, welches das Gewicht ist, mit dem der Patient die Übung maximal 10 Mal ausführen kann.
Anhand des Anamnesegespräches und des Assessments wird dann ein individueller Behandlungsplan erstellt. Hierfür werden gemeinsam Ziele formuliert. Hierbei sind sowohl langfristige Ziele als auch kurzfristige Ziele für die einzelnen Phasen der Behandlung wichtig. Für den Behandlungsplan wählen wir aus verschiedenen Behandlungsansätzen, die im folgenden für sie vorgestellt werden.
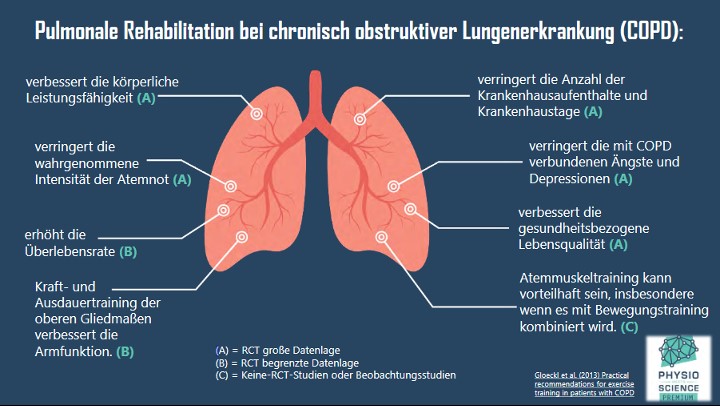
Das Ziel einer Lungenrehabilitation ist die Verbesserung der Übungskapazität, Leistungsfähigkeit und Belastbarkeit und dadurch auch der Lebensqualität, sowie das Reduzieren von Exazerbationen und Sterblichkeit. Hierfür wird eine Kombination aus Krafttraining, Intervalltraining und Ausdauertraining empfohlen. Mehrere Studien zeigen, dass eine Kombination dieser Trainingsmethoden einen grossen Einfluss haben auf die Lebensqualität, Belastbarkeit, physische Leistung, Reduktion von Kurzatmigkeit, Reduktion von Krankenhausaufenthalten und Sterblichkeit sowie die Reduktion von Angst und Depressionen. 17, 18, 19, 20, 21
Beim Krafttraining liegt der Fokus auf einem Oberkörpertraining. Verbesserte Kraft in den Armen bewirkt auch eine bessere Ausdauer und Belastbarkeit für Aktivitäten des Oberkörpers under Arme. 12 Es wird aber insgesamt ein Training der allgemeinen Muskulatur der oberen und unteren Gliedmassen empfohlen. 12
Wie oben beschrieben, vermindert sich die Kraft der Atemmuskulatur. Die Muskeln sind oft stark überbelastet, da sie mehr Kraft aufwenden müssen, um die Atmung zu unterstützen. Daher ist ein Training dieser Muskeln sehr wichtig, um diese belastbar zu machen.
Edukation & Selbstmanagement
In der Behandlung von COPD ist ein gutes Selbstmanagement die beste Grundlage für die Therapie. Dem Patienten wird deutlich gemacht, wie er sein sein Verhalten und seinen Lebensstil optimieren kann, um die Risikofaktoren für eine Verschlechterung des Krankheitsverlaufes zu minimieren und die Lebensqualität zu steigern. Des weiteren ist es wichtig, dass der Patient lernt, Exazerbationen rechtzeitig zu erkennen, während des Trainings auf seinen Körper zu hören, seine Belastungsgrenzen zu erkennen, Entscheidungen zu treffen, wann Hilfe geholt werden sollte und persönliche Ziele zu formulieren.
Ernährung 30
Wie oben geschrieben, geht eine Erkrankung an COPD einher mit starkem Gewichtsverlust und Verlust an Muskelmasse. Dies geschieht durch einen erhöhten Energiebedarf, den die chronisch entzündlichen Prozesse und die überlastete Atemmuskulatur durch die geschädigte Lunge haben. Der Körper baut durch den Energiemangel zunehmend Muskeleiweiss ab, um die verloren gegangene Energie zurück zu gewinnen, wodurch es aber zum Abbau von Muskelmasse kommt.
Um dies vorzubeugen, ist die richtige Ernährung ein wichtiger Bestandteil der Behandlung und kann bei Bedarf von unserer Ernährungsberaterung gecoacht und begleitet werden. Studien zeigen ausserdem, dass der Ernährungszustand und die Sterblichkeit im klaren Zusammenhang stehen. Untergewicht reduziert die durchschnittliche Überlebenszeit und ein verbessertes Gewicht verlängert das Überleben. Im Allgemeinen ist es wichtig, auf eine vollwertige und bei Untergewicht hochkalorische Ernährung zu achten und vor allem eine gute Eiweisszufuhr einzuhalten, die essentiell für Muskelerhalt und -aufbau ist. Studien belegen gute Ergebnisse bei der Zufuhr von Trinknahrung zwei- bis dreimal täglich zusätzlich zu den Mahlzeiten. Wichtig ist ebenfalls eine ausreichende Flüssigkeitszufuhr, um das Abhusten zu erleichtern.
In Ruhe mehrere kleine, statt wenige grosse Mahlzeiten über den Tag verteilt sind bekömmlicher. Ausreichend Vitamine, Omega-3-Fettsäuren (eventuell als Nahrungsergänzungsmittel) und Kalzium sind wichtig für COPD-Patienten. Ebenso wie reichlich Obst, Gemüse und Vollkornprodukte. Alkoholische Getränke sollten vermieden werden, da sie die Harnsäurekonzentration im Blut erhöhen. Harnsäure kann zu einer Verschlechterung von COPD führen, da sie die Lungenfunktion und die körperliche Belastbarkeit reduziert. Es entstehen dadurch vermehrte Exazerbationen und Begleiterkrankungen.
Atemtherapie 15
Es gibt einige Techniken bei der Atmung, die die Atemnot reduzieren können und die Atmung bei Belastung verbessern können. Des weiteren können Atemtechniken gegen Angst und Panik helfen sowie bei der Entfernung von Sekret.
Die Lippenbremse ist eine Atemtechnik, um während Anstrengung die Atemfrequenz und Atemnot zu senken und die Erholung zu beschleunigen. Ebenfalls ist eine gute Kontrolle über die Geschwindigkeit der Atmung wichtig. Weitere Faktoren sind eine entspannte, langsame, tiefe Atemtechnik zu erlernen, sowie eine gute Haltung oder Lagerung dabei. Entspannungsstrategien können helfen, Panik und Angst bei Kurzatmigkeit zu reduzieren.
Atemwegsreinigungstechniken
Es gibt verschiedene Atemwegsreinigungstechniken, die dazu dienen, die Lunge zu belüften, die Durchblutung zu fördern und das Sekret zu mobilisieren. 15 Die Techniken beinhalten sowohl manuelle Techniken und Haltungsdrainagen, die durch den Therapeuten ausgeführt werden, als auch Techniken, die dem Patienten angelernt werden können, damit diese selbständig durchgeführt werden. Hierunter fallen zum Beispiel:
- Autogene Drainage: Durch Tiefatemübungen, auch in Verbindungen mit Lagerungen und Brustkorbbewegungen, wird Luft hinter das Sekret in den kleinen und mittleren Atemwegen gebracht.
- Huffing: eine Husttechnik das dabei hilft effektiver zu husten, ohne sich sehr zu ermüden.
- das Erlernen eines Atemzirkels
Ausserdem gibt es verschiedene PEP (Positive Expiratory Pressure) Geräte (siehe Bild hier unten) bei denen meist gegen Widerstand ausgeatmet werden muss, wodurch Vibrationen entstehen, die den Bronchialschleim lösen. Des weiteren kann laut einer aktuellen Studie durch ein regelmässiges Training, von 5 – 7 Mal 5 – 20 Minuten, mit diesen Geräten die Atemausdauer um 86%, die Lebensqualität um 21% und die Einatemmuskulatur um 55% verbessert werden. 29

Krafttraining
Ziel des Krafttrainings ist es, eine Reduzierung von COPD bedingten, körperlichen Einschränkungen zu erreichen. Im Vergleich zu einem Ausdauertraining, ist die Kurzatmigkeit beim Krafttraining die Kurzatmigkeit weniger ein einschränkender Faktor.
Es wird ein Muskeltraining für den Ober- und Unterkörper empfohlen. Hierfür wird die Belastung mit der Zeit langsam gesteigert zwischen 50 – 80% des 1 RM. Das 1 RM, auch die Maximalkraft genannt, ist das Gewicht, mit dem man die jeweilige Übung nur 1 Mal ausführen kann. Sobald der Patient 1 – 2 Wiederholungen mehr durchführen kann als 6 – 12 Wiederholungen, kann das Gewicht um 2 – 10% gesteigert werden.
Ausserdem ist bei uns, bei einer stark eingeschränkten, körperlichen Belastbarkeit, ein Bloodflow Restriction Training möglich, wodurch nur bei 30% der Maximalkraft, die gleichen Trainingseffekte erzielt werden können. Mithilfe von sicheren Bändern wird der Blutfluss während des Trainings leicht eingeschränkt. Der Blutfluss wird somit reduziert und dadurch die Ausschüttung von Wachstumshormonen angeregt.
Des weiteren ist ein Krafttraining der Einatemmuskulatur wichtig. 22, 23 Dies sollte 5 – 7 Mal die Woche durchgeführt werden für 5 – 20 Minuten. Hierbei können verschiedene Atemtrainer gebraucht werden, die im Abschnitt Atemtechniken erläutert und vorgestellt werden.
Quellenangabe
- Agustí, A., Vogelmeier, C., & Faner, R. (2020). COPD 2020: changes and challenges. American Journal of Physiology-Lung Cellular and Molecular Physiology, 319(5), L879-L883.
- Salvi, S. S., & Barnes, P. J. (2009). Chronic obstructive pulmonary disease in non-smokers. The lancet, 374(9691), 733-743.
- Gupta, N., Malhotra, N., & Ish, P. (2021). GOLD 2021 guidelines for COPD—what’s new and why. Advances in respiratory medicine, 89(3), 344-346.
- Vogelmeier, C. F., Criner, G. J., Martinez, F. J., Anzueto, A., Barnes, P. J., Bourbeau, J., … & Agusti, A. (2017). Global strategy for the diagnosis, management, and prevention of chronic obstructive lung disease 2017 report. GOLD executive summary. American journal of respiratory and critical care medicine, 195(5), 557-582.
- Silva, G. E., Sherrill, D. L., Guerra, S., & Barbee, R. A. (2004). Asthma as a risk factor for COPD in a longitudinal study. Chest, 126(1), 59-65.
- World Health Organization. (1997). α_1-antitrypsin deficiency: Memorandum from a WHO meeting. Bull World Health Organ, 75, 397-415.
- van Eerd, E. A., van der Meer, R. M., van Schayck, O. C., & Kotz, D. (2016). Smoking cessation for people with chronic obstructive pulmonary disease. Cochrane Database of Systematic Reviews, (8).
- Wongsurakiat, P., Maranetra, K. N., Wasi, C., Kositanont, U., Dejsomritrutai, W., & Charoenratanakul, S. (2004). Acute respiratory illness in patients with COPD and the effectiveness of influenza vaccination: a randomized controlled study. Chest, 125(6), 2011-2020.
- Poole, P., Chacko, E. E., Wood-Baker, R., & Cates, C. J. (2006). Influenza vaccine for patients with chronic obstructive pulmonary disease. Cochrane Database of Systematic Reviews, (1).
- Huang, C. L., Nguyen, P. A., Kuo, P. L., Iqbal, U., Hsu, Y. H. E., & Jian, W. S. (2013). Influenza vaccination and reduction in risk of ischemic heart disease among chronic obstructive pulmonary elderly. Computer methods and programs in biomedicine, 111(2), 507-511.
- Pauwels, R. A., Löfdahl, C. G., Laitinen, L. A., Schouten, J. P., Postma, D. S., Pride, N. B., & Ohlsson, S. V. (1999). Long-term treatment with inhaled budesonide in persons with mild chronic obstructive pulmonary disease who continue smoking. New England Journal of Medicine, 340(25), 1948-1953.
- Velloso, M., do Nascimento, N. H., Gazzotti, M. R., & Jardim, J. R. (2013). Evaluation of effects of shoulder girdle training on strength and performance of activities of daily living in patients with chronic obstructive pulmonary disease. International journal of chronic obstructive pulmonary disease, 8, 187.
- Seemungal, T. A., Donaldson, G. C., Bhowmik, A., Jeffries, D. J., & Wedzicha, J. A. (2000). Time course and recovery of exacerbations in patients with chronic obstructive pulmonary disease. American journal of respiratory and critical care medicine, 161(5), 1608-1613.
- Seemungal, T. A., Donaldson, G. C., Paul, E. A., Bestall, J. C., Jeffries, D. J., & Wedzicha, J. A. (1998). Effect of exacerbation on quality of life in patients with chronic obstructive pulmonary disease. American journal of respiratory and critical care medicine, 157(5), 1418-1422.
- Bott, J., Blumenthal, S., Buxton, M., Ellum, S., Falconer, C., Garrod, R., … & White, J. (2009). Guidelines for the physiotherapy management of the adult, medical, spontaneously breathing patient. Thorax, 64(Suppl 1), i1-i52.
- Gloeckl, R., Marinov, B., & Pitta, F. (2013). Practical recommendations for exercise training in patients with COPD. European Respiratory Review, 22(128), 178-186.
- Gosselink, R. I. K., Troosters, T., & Decramer, M. (1996). Peripheral muscle weakness contributes to exercise limitation in COPD. American journal of respiratory and critical care medicine, 153(3), 976-980.
- Hamilton, A. L., Killian, K. J., Summers, E., & Jones, N. L. (1995). Muscle strength, symptom intensity, and exercise capacity in patients with cardiorespiratory disorders. American journal of respiratory and critical care medicine, 152(6), 2021-2031.
- Troosters, T., Casaburi, R., Gosselink, R., & Decramer, M. (2005). Pulmonary rehabilitation in chronic obstructive pulmonary disease. American journal of respiratory and critical care medicine, 172(1), 19-38.
- O’Shea, S. D., Taylor, N. F., & Paratz, J. D. (2009). Progressive resistance exercise improves muscle strength and may improve elements of performance of daily activities for people with COPD: a systematic review. Chest, 136(5), 1269-1283.
- Simpson, K., Killian, K., McCartney, N., Stubbing, D. G., & Jones, N. L. (1992). Randomised controlled trial of weightlifting exercise in patients with chronic airflow limitation. Thorax, 47(2), 70.
- Gosselink, R., De Vos, J., Van Den Heuvel, S. P., Segers, J., Decramer, M., & Kwakkel, G. (2011). Impact of inspiratory muscle training in patients with COPD: what is the evidence?. European Respiratory Journal, 37(2), 416-425.
- Lötters, F., Van Tol, B., Kwakkel, G., & Gosselink, R. (2002). Effects of controlled inspiratory muscle training in patients with COPD: a meta-analysis. European Respiratory Journal, 20(3), 570-577.
- Brashier, B. B., & Kodgule, R. (2012). Risk factors and pathophysiology of chronic obstructive pulmonary disease (COPD). J Assoc Physicians India, 60(Suppl), 17-21.
- Fabbri, L. M., Luppi, F., Beghé, B., & Rabe, K. F. (2008). Complex chronic comorbidities of COPD. European Respiratory Journal, 31(1), 204-212.
- Kabitz, H. J., & Windisch, W. (2007). Diagnostik der Atemmuskelfunktion: state of the art. Pneumologie, 61(09), 582-587.
- de Oca, M. M., Torres, S. H., Gonzalez, Y., Romero, E., Hernández, N., Mata, A., & Tálamo, C. (2006). Peripheral muscle composition and health status in patients with COPD. Respiratory medicine, 100(10), 1800-1806.
- Celli, B. R., Cote, C. G., Marin, J. M., Casanova, C., Montes de Oca, M., Mendez, R. A., … & Cabral, H. J. (2004). The body-mass index, airflow obstruction, dyspnea, and exercise capacity index in chronic obstructive pulmonary disease. New England Journal of Medicine, 350(10), 1005-1012.
- Belli, S., Prince, I., Savio, G., Paracchini, E., Cattaneo, D., Bianchi, M., … & Balbi, B. (2021). Airway clearance techniques: the right choice for the right patient. Frontiers in medicine, 8, 544826.
- Steinkamp, G. (2003). COPD, die Systemerkrankung: Ernährung: zu wenig beachtet und noch ungelöst. Pneumologie, 57(11), 681-689.